43
参考文献 44
1 绪论
1.1 概述
1.1.1 研究背景
丙型肝炎病毒(HCV)是一种主要通过血液传播的病原体,是慢性肝病、肝移植的主要病因[1]。丙型肝炎病毒的慢性感染可导致肝脏慢性坏死和纤维化,部分患者可能发展为肝硬化甚至发生癌变(HCC)[2]。据世界卫生组织(WHO)统计,2000年全球已有超过1.7亿人感染HCV病毒,占世界人口总数的3%,每年新发感染者300~400万[3]。有报道指出,我国已有超过3000万的HCV感染者,并有明显的上升趋势[4]。HCV感染后大约10%-20%的患者在10~30年内发展为肝硬化,每年约1%~5%的肝硬化患者发展成肝细胞癌(HCC)[5]。尽管重组干扰素-α(IFN-α)在治疗慢性丙型肝炎(CHC)上取得了可喜的成绩,但目前主要的治疗方案——聚乙二醇干扰素-α(PEG-IFN-α)联合利巴韦林(RBV)对基因Ⅰ型患者的有效率仍然只有50%[5]。并且,这种治疗方案价格昂贵并且副作用大。2011年5月,HCV蛋白酶抑制剂伯赛匹韦(Victrelis)和特拉普韦(Incivek)的问世给人们带来新的希望,但它们对治疗过程的具体影响目前尚不清楚,与重组干扰素和利巴韦林联用后的持续病毒学反应只有70~80%。由此可见,选择合理的药物靶点、研发高效的抗HCV药物成为目前亟待解决的问题。源[自[751``论`文]网·www.751com.cn/
目前,丙型肝炎病毒(HCV)编码的非结构蛋白5A(NS5A)成为抑制肝炎病毒、研发抗病毒药物的新目标。尽管NS5A蛋白在HCV病毒复制周期中的具体功能尚不明确,但它在宿主细胞和病原体的多数活动如RNA复制、病毒颗粒的装配及宿主细胞的免疫反应中均有重要影响。磷酸化的 NS5A 与病毒的复制关系密切,它与病毒的产生和释放有关,并且能够通过影响病毒与宿主细胞的相互作用,干扰细胞内重要的信号通路,影响免疫系统和细胞周期,最终促使 与HCV 相关的慢性肝病的发生与发展[7]。
1.2.2 BMS-790052
1.1.2.1 BMS-790052的结构及功能
BMS-790052是一种HCV NS5A蛋白抑制剂。其结构式如下:
小分子药物BMS-790052通过改变NS5A在复制复合体中的定位而抑制HCV的复制[8]。该药物的Ⅱ期临床试验结果显示:使用NS5A蛋白抑制剂BMS-790052联合聚乙二醇干扰素和利巴韦林治疗基因Ⅰ型初治慢性丙肝患者,治疗12周后持续病毒学应答率可达92%[9]。论文网
BMS-790052证实了NS5A蛋白这一新的药物靶点在丙肝临床治疗中的有效性,它同时为设计选择性更强、细胞毒性更低的第二代抑制剂提供依据。我们可以将BMS-790052的分子结构划分为四个重要区域(如图1.1所示):Ⅰ区(联苯部分),Ⅱ区(咪唑环部分),Ⅲ区(脯氨酸部分结构),Ⅳ区(氨基酸及其“帽”结构)。由于该结构中的Ⅰ区和Ⅳ区已被广泛研究,因此目前研究人员主要把目光集中在对Ⅱ区和Ⅲ区的研究上。其中,Ⅱ区的咪唑环易于卤化,这将有助于采用过渡金属催化交叉偶联的方法制备更为复杂的相似结构的化合物;Ⅲ区的脯氨酸结构可用其他脯氨酸类似物进行转换[10]。
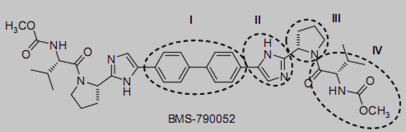
图1.1 BMS-790052分子结构区域划分
1.1.2.2 BMS-790052的主要合成方法
该化合物属于对称结构,目前主要有两种合成思路:一种是以联苯为原料,采用对称法合成,但往往在合成过程中一取代产物较易生成,反应速率较快,严格控制反应条件,如延长反应时间或升高温度等方法可得到产率较高的二取代产物(见图1.2);另一种方法是先合成该对称结构的一半,再采用偶联的方法将结构片段重组,从而获得目标产物联苯衍生物(见图1.3)。由于第一种合成路线反应的类型较为常见,对应单元反应的工业化生产方法较为成熟,故本文主要对第一种合成路线进行讨论,并优化其反应条件。 BMS-790052的合成工艺优化(3):http://www.751com.cn/yixue/lunwen_71385.html

